Équipes
Équipe HeLip
L’équipe « Hepatitis Viruses and Liver Pathogenesis » (HeLiP) a pour objectif de comprendre les mécanismes de la persistance virale et de la pathogénie hépatique afin d’identifier de nouveaux biomarqueurs et de nouvelles cibles thérapeutiques.
Elle s’articule autour de deux axes principaux :
- Axe I. Pathogénie des maladies du foie, décompensation et prédisposition au carcinome hépatocellulaire (CHC)
- Axe II. Éradication des hépatites B et D : compréhension de la persistance virale pour identifier des cibles innovantes

Contexte
Le carcinome hépatocellulaire (CHC) est le 5ᵉ cancer le plus fréquent dans le monde et se classe au 3ᵉ rang en termes de mortalité par cancer.
À l’échelle mondiale, les infections chroniques par les virus de l’hépatite B (VHB) et de l’hépatite C (VHC) sont les principales causes de maladies hépatiques menant au CHC, tandis que la co-infection par le virus de l’hépatite Delta (VHD) accélère significativement la progression de la maladie. La maladie hépatique liée à l’alcool (ALD) et la stéatose hépatique métabolique (MASLD) sont des causes fréquentes et croissantes de CHC, notamment dans les pays occidentaux. L’infection chronique par le VHB est la première cause de CHC et un problème majeur de santé publique, étant la maladie infectieuse chronique la plus répandue dans le monde, avec plus de 296 millions de personnes concernées. La résolution clinique de l’infection par le VHB nécessiterait le contrôle des génomes viraux persistants et des cellules infectées résiduelles par le système immunitaire, ce qui est rarement atteint avec les traitements standards actuels. Bien que la récente révolution thérapeutique ait permis de guérir la majorité des patients atteints d’une infection chronique par le VHC, le risque résiduel observé de développement d’un CHC après guérison doit être entièrement caractérisé. Les mécanismes possibles impliqués dans le CHC induit par le VHC incluent le remodelage du métabolisme hépatique, le stress cellulaire chronique, l’inflammation et d’autres modulations des voies de signalisation cellulaire, qui peuvent également être informatifs pour la MASLD et l’ALD. De plus, les comorbidités comme la MASLD et l’ALD, dont la prévalence est croissante, surtout dans les pays développés, augmentent le risque de complications hépatiques (cirrhose, CHC, décompensation hépatique).
Dans ce contexte, nous capitalisons sur notre expertise et notre programme de recherche translationnelle et clinique solide, s’appuyant sur de nombreuses cohortes de patients nationales et internationales et des essais cliniques, pour nous concentrer sur deux grands axes :
Axe I. Pathogénie des maladies du foie, décompensation et prédisposition au CHC
Axe II. Élimination de l’hépatite B et Delta : comprendre la persistance virale pour découvrir des cibles innovantes
Axe I. Pathogénie des maladies du foie, décompensation et prédisposition au Carcinome Hépato-Cellulaire
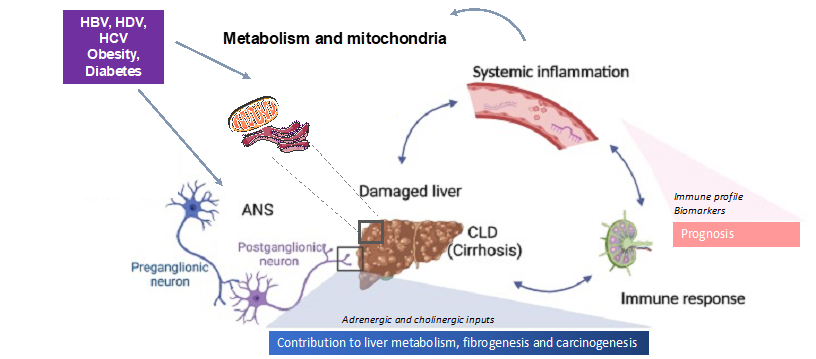
En nous appuyant sur notre expertise en pathologie moléculaire des hépatites virales, nous recherchons les dénominateurs communs des pathologies à l’origine des hépatites chroniques B/C/D, de l’ALD et de la MASLD. Dans toutes ces étiologies, les flux métaboliques altérés, le stress oxydatif, l’inflammation et les altérations des signaux cellulaires contribuent à la progression vers des maladies hépatiques sévères. Dans les maladies du foie en phase terminale (maladies chroniques hépatiques avancées compensées, décompensations aiguës avec ou sans défaillance d’organe), la progression de la maladie, le dysfonctionnement immunitaire et la défaillance multi-organes sont en partie entraînés par l’inflammation. Le rôle de l’innervation dans la progression des maladies hépatiques graves, en particulier dans la pathogénie du CHC, commence à être dévoilé grâce à nos travaux. L’identification de cibles moléculaires, de voies de signalisation ou de conditions inflammatoires communes, modulées ou non par le système nerveux, devrait permettre de développer de nouveaux outils pour répondre à des enjeux cliniques actuels tels que des modèles pronostiques individualisés robustes et de nouvelles options thérapeutiques pour la fibrose, l’insuffisance hépatique et le CHC.
Objectifs :
Nous allons explorer le rôle des voies métaboliques, inflammatoires et neurohépatiques dans les maladies chroniques du foie à différents stades, afin d’identifier et/ou caractériser des voies pouvant servir de biomarqueurs pronostiques ou de nouvelles cibles thérapeutiques, à travers trois objectifs spécifiques :
- Objectif spécifique n°1 (HeLiP). Rôle des altérations métaboliques et du stress oxydatif induits par les virus dans les maladies hépatiques liées au VHC et VHB/VHD
- Objectif spécifique n°2 (HeLiP). Contribution neuronale au métabolisme hépatique, à la fibrogenèse et à la cancérogenèse
- Objectif spécifique n°3 (HeLiP + EpiLiv). Rôle de l’inflammation dans les maladies hépatiques en phase terminale (ESLD) et sa contribution aux complications de la cirrhose et à la mauvaise évolution
Axe II. Élimination de l’hépatite B et Delta : comprendre la persistance virale pour découvrir des cibles innovantes

Les traitements actuels contre l’hépatite B chronique permettent de supprimer la réplication virale mais nécessitent un traitement à vie dans la majorité des cas, car ils ne peuvent pas éliminer l’ADNccc, matrice nucléaire pour la réplication virale. Cet ADNccc, chromatinisé et régulé par des mécanismes épigénétiques, est responsable de la persistance virale et des rechutes après arrêt du traitement. De plus, la capacité du VHB à s’intégrer dans le génome de l’hôte rend difficile l’atteinte d’une guérison complète. La réplication virale résiduelle, la production d’antigènes et la persistance des génomes viraux nucléaires contribuent de manière significative au risque de CHC, même chez les patients sous traitement avec suppression virale. De nouvelles approches thérapeutiques sont nécessaires pour éradiquer ou « silencier » l’ADNccc afin de permettre des traitements de durée finie, élargissant ainsi l’accès au traitement à tous les porteurs du VHB. La reprogrammation de l’environnement microhépatique sera également clé pour rétablir un contrôle immunitaire durable. Des combinaisons d’antiviraux à action directe et de modulateurs immunitaires sont actuellement en cours d’évaluation clinique. Le développement de ces nouvelles approches combinatoires nécessite l’identification de nouveaux critères d’évaluation et de biomarqueurs non-invasifs de l’ADNccc intra-hépatique.
Environ 15 millions de porteurs chroniques du VHB sont également co-infectés par le VHD, ce qui entraîne une progression accélérée vers la cirrhose et le CHC. La gestion des patients co-infectés est limitée par la faible efficacité de l’interféron. Des traitements efficaces contre le VHD sont donc urgents : à ce jour, seul le Bulevirtide, un inhibiteur de l’entrée virale, a obtenu une autorisation conditionnelle de l’EMA, tandis que d’autres inhibiteurs sont en phase II d’essais cliniques.
Objectifs :
- Objectif spécifique n°1 (HeLiP). Générer de nouvelles connaissances sur la biologie de l’ADNccc, notamment sur les étapes clés de sa formation et de sa régulation transcriptionnelle, in vitro et in vivo
- Objectif spécifique n°2 (HeLiP). Identifier de nouvelles cibles ou approches pour dégrader ou inactiver fonctionnellement (« silencier ») le pool d’ADNccc
- Objectif spécifique n°3 (HeLiP + EpiLiv). Caractériser et évaluer des biomarqueurs sériques non-invasifs reflétant la quantité et l’activité transcriptionnelle de l’ADNccc hépatique, in vitro et in vivo, chez des patients VHB seuls ou co-infectés VHB-VHD
- Objectif spécifique n°4 (HeLiP + EpiLiv). Évaluer de nouvelles approches thérapeutiques dans des modèles expérimentaux et dans des essais cliniques
- Objectif spécifique n°5 (HeLiP). Évaluer l’impact de la variabilité des génomes VHB et VHD dans différentes régions du monde sur l’évolution de la maladie hépatique et la réponse aux traitements
Présentation de l'équipe
L’équipe « Hepatitis Viruses and Liver Pathogenesis » (HeLiP) a pour objectif de comprendre les mécanismes de la persistance virale et de la pathogénie hépatique afin d’identifier de nouveaux biomarqueurs et de nouvelles cibles thérapeutiques.
Investigateurs principaux : B. Bartosch (DR), I. Chemin (DR), F. Lebossé (MCUPH), B. Grigorov (MCU), R. Parent (CR), C. Scholtes (MCUPH), B. Testoni (CR), F. Zoulim (PUPH)
ITA titulaires : I. Bordes (Tech), E. Combe (IE), M. Michelet (IE), J. Molle (IE)
Autres membres : 7 post-doctorants, 5 doctorants, 5 ITA sous contrat
Financements: Labex DevWeCan et HumanToCan (changements métaboliques et régulation neuronale dans le CHC), ANRS (VDAC, HDV, netrine-4 & VHC), IRP HepDelta Mongolie (HDV), SNFGE (FARE 2021), HCL (Jeune Chercheur 2018), INCa PLBio (ciblage neuronal dans le CHC), Inserm/INCa PCSI (caractérisation d’un composé indole-éthanamine à activité anti-CHC), Cancéropôle CLARA (évaluation préclinique du ciblage de la nétrine-1 dans les maladies hépatiques chroniques), H2020 IP-cure-B (« profilage immunitaire pour guider des interventions dirigées contre l’hôte afin de guérir les infections à VHB »), Beam Therapeutics (édition de base), Blue Jay (anticorps neutralisant).
Projets
Publications
2025
- Fernandes P, Wang Y, Doisne JM, Thaller A, Fiquet O, Dailleux R, Amblard F, Testoni B, Aronthippaitoon Y, Mouquet H, Sureau C, Reyné B, Tiezzi C, Soussan P, Levrero M, Zoulim F, Schinazi RF, Strick-Marchand H. Functional immune responses induced by a capsid assembly modulator in chronic hepatitis B virus-infected humanized mice. Cell Host Microbe. 2025 Dec 23:S1931-3128(25)00497-4. doi: 10.1016/j.chom.2025.12.001. Epub ahead of print. PMID: 41443190.
- Begré L, Zoulim F, Boyd A. Hepatitis B virus functional cure in persons with HIV: what are the predictors and which novel markers are useful? Curr Opin HIV AIDS. 2025 Dec 18. doi: 10.1097/COH.0000000000001002. Epub ahead of print. PMID: 41417916.
- Giraud G, Testoni B. Role of cccDNA in the Quest for HBV Cure- Implications for HIV-HBV Coinfection. Curr HIV/AIDS Rep. 2025 Dec 17;22(1):57. doi: 10.1007/s11904-025-00766-9. PMID: 41405783.
- Zhang BH, Zhou Y, Horrigan S, Luckenbaugh L, Hu J, Zoulim F, Zhang YY. HBVZ10, an AAV8 vector-based new HBV therapy candidate for cccDNA elimination. Mol Ther Methods Clin Dev. 2025 Nov 19;33(4):101646. doi: 10.1016/j.omtm.2025.101646. PMID: 41404410; PMCID: PMC12704295.
- Furquim d’Almeida A, Vanderlinden A, Bourgeois S, Mulkay JP, Sersté T, Struyve M, Deressa B, Sprengers D, de Vos M, Callens J, Shihao B, Reynaert H, Deltenre P, Janssens F, Negrin-Dastis S, Stärkel P, Orlent H, Van Roey G, Verhelst X, Moreno C, Delwaide J, Van Steenkiste C, Verlinden W, Colle I, Plissonnier ML, Mukadi BK, Testoni B, Zoulim F, Matheeussen V, Vanwolleghem T. Clinical Trial: Hepatitis B Virus Genotype and a Combination of End-of-Treatment Biomarkers Predict Severe Flares After Nucleos(t)ide Analogue Cessation. Aliment Pharmacol Ther. 2025 Nov 19. doi: 10.1111/apt.70465. Epub ahead of print. PMID: 41261561.
- Stern C, Loustaud-Ratti V, Yurdaydin C, Brancaccio G, Jachs M, Reiberger T, Bardou-Jacquet E, Metivier S, Alric L, Colombain L, Meszaros M, Mathurin P, Yardeni D, Etzion O, Neumann-Haefelin C, Douglas M, Poulin S, Bazinet M, Metin RO, Vitale A, Gaeta GB, Schwarz M, Ben-Ali S, Bedoya JU, Testoni B, Zoulim F, Plissonnier ML, Levrero M, Paradis V, Francois S, de Freitas C, Kaysin F, Lecomte L, Morvan C, Schramko J, Bondezi K, Baril MÉ, Brichler S, Gerber A, Gordien E, Mackiewicz V, Dahari H, Svicher V, Chevaliez S, Vaillant A, Bourliere M. Safety and efficacy of REP 2139-Mg in patients with HDV-related advanced liver disease in an international compassionate access program. J Hepatol. 2025 Nov 6:S0168-8278(25)02612-1. doi: 10.1016/j.jhep.2025.10.029. Epub ahead of print. PMID: 41205755.
- Dongelmans EJ, Patmore LA, Lim SG, Bourliere M, Jiang S, Ganne-Carrie N, Brouwer WP, Feld JJ, Huang Y, Carrion JA, Broquetas T, Hu Q, Fung S, Carrat F, Zoulim F, Hansen BE, Xie Q, Janssen HLA, Sonneveld MJ. HBsAg decline and clearance with peg-IFN therapy added to nucleos(t)ide analogues: an individual participant data meta-analysis of prospective trials (PROSPER). Gut. 2025 Nov 5:gutjnl-2025-336251. doi: 10.1136/gutjnl-2025-336251. Epub ahead of print. PMID: 41198171.
- Zhang B-H, Zhou Y, Horrigan S, Zoulim F, Hu J, Zhang Y-Y. Replication-driven HBV cccDNA loss in chimeric mice with humanized livers. J Virol. 2025 Nov 25;99(11):e0129525. doi: 10.1128/jvi.01295-25. Epub 2025 Nov 6. PMID: 41196060; PMCID: PMC12645921.
- Cornberg M, Zoulim F, Gish R, Jacobson IM, Kushner T, Lampertico P, Rizzetto M, Yurdaydin C, Manns M. Best practices for screening, testing, diagnosing, and treating patients with hepatitis D (delta) virus based on global expert review and recent guidelines. Antivir Ther. 2025 Oct;30(4):13596535251349380. doi: 10.1177/13596535251349380. Epub 2025 Sep 29. PMID: 41024346.
- European Association for the Study of the Liver. EASL Clinical Practice Guidelines on the management of hepatitis B virus infection. J Hepatol. 2025 Aug;83(2):502-583. doi: 10.1016/j.jhep.2025.03.018. Epub 2025 May 10. PMID: 40348683.
- Kennedy PT, Allweiss L, Bertoletti A, Cornberg M, Gehring AJ, Guidotti LG, Kerth HA, Lemoine M, Levrero M, Lim SG, Tavis JE, Testoni B, Tu T; International Coalition to Eliminate HBV. Scientific and medical evidence informing expansion of hepatitis B treatment guidelines. Lancet Gastroenterol Hepatol. 2025 Oct;10(10):941-951. doi: 10.1016/S2468-1253(25)00053-6. Epub 2025 Jul 23. PMID: 40714040.
- Degasperi E, Sandmann L, Wedemeyer H, Lampertico P; Delta Cure 2024 Working Group. Hepatitis D Virus Infection: Pathophysiology, Epidemiology and Treatment. Report From the Third Delta Cure Meeting 2024. Liver Int. 2025 Jul;45(7):e70189. doi: 10.1111/liv.70189. PMID: 40540405.
- Khomich OA, Giavalisco P, Parent R, Krasnov GS, Tessarz P, Meuleman P, Burm R, Zakirova NF, Molle J, Batbold E, Gottlieb E, Zoulim F, Ivanov AV, Bartosch B. IFN-β production promotes metabolic rewiring and protection against oxidative stress in hepatitis delta virus-infected hepatocyte cultures. Cell Death Dis. 2025 Jul 18;16(1):534. doi: 10.1038/s41419-025-07838-z. PMID: 40681530; PMCID: PMC12274286.
- Lotto M, Ramier C, Carrat F, Périères L, Delaroque-Astagneau E, Nicol J, Marcellin F, Zoulim F, Di Beo V, Bertheau M, Pol S, Protopopescu C, Bourlière M, Carrieri P; ANRS/AFEF CO22 HEPATHER Study Group. Mortality risk in migrant and non-migrant individuals with chronic hepatitis B virus infection: a French hospital-based cohort study (ANRS CO22 HEPATHER). BMC Glob Public Health. 2025 Jul 1;3(1):58. doi: 10.1186/s44263-025-00173-7. PMID: 40598581; PMCID: PMC12220402.
- Feld JJ, Gehring AJ, Zoulim F. Getting to HBV cure-Will new biomarkers help? Hepatology. 2025 Apr 1. doi: 10.1097/HEP.0000000000001334. Epub ahead of print. PMID: 40168396.
- Roca Suarez AA, Jühling F, Moehlin J, Mailly L, Virzì A, Brignon N, Durand SC, Oudot MA, Schaeffer E, Martin R, Meiss-Heydmann L, Bach C, Boulahtouf Z, Girard L, Osswald E, Jamey C, Brumaru D, Dali-Youcef N, Mukherji A, Saez-Palma M, Testoni B, Zoulim F, Koneru B, Fujiwara N, Hoshida Y, Felli E, Pessaux P, Tremblay ML, Parent R, Schuster C, Baumert TF, Lupberger J. Protein tyrosine phosphatase delta is a STAT3-phosphatase and suppressor of metabolic liver disease. eGastroenterology. 2025 Jan 27;3(1):e100159. doi: 10.1136/egastro-2024-100159. PMID: 40124988; PMCID: PMC11927410.
- Ramier C, Protopopescu C, Di Beo V, Parlati L, Marcellin F, Carrat F, Asselah T, Bourlière M, Carrieri P; ANRS/AFEF CO22 HEPATHER Study Group. Behaviour-Based Predictive Scores of Hepatocellular Carcinoma in People With Chronic Hepatitis B (ANRS CO22 HEPATHER). Liver Int. 2025 Apr;45(4):e70065. doi: 10.1111/liv.70065. PMID: 40087922; PMCID: PMC11909585.
- Nahon P, Lusivika-Nzinga C, Merle P, Zoulim F, Decaens T, Ganne-Carrié N, Pageaux GP, Leroy V, Alric L, Bronowicki JP, Bourlière M, Gournay J, Tran A, Pol S, Mathurin P, Loustaud-Ratti V, Métivier S, De Ledinghen V, Abergel A, Thabut D, D’Alteroche L, Bouattour M, Asselah T, Ouzan D, Cales P, Chazouillères O, Gelu-Simeon M, Roulot D, Boursier J, Cagnot C, Tamazirt S, Pascale A, Nilusmas S, Lewin M, Ziol M, Carrat F, Duclos-Vallée JC; ANRS CO12 CirVir, CO22 Hepather, and LICAVIR groups. Value of non-invasive test dynamics in guiding HCC surveillance decisions after HCV cure in patients with cirrhosis. J Hepatol. 2025 Sep;83(3):701-711. doi: 10.1016/j.jhep.2025.02.008. Epub 2025 Feb 26. PMID: 40020929.
- Nahon P, Lusivika-Nzinga C, Merle P, Zoulim F, Decaens T, Ganne-Carrié N, Pageaux GP, Leroy V, Alric L, Bronowicki JP, Bourlière M, Gournay J, Tran A, Pol S, Mathurin P, Loustaud-Ratti V, Métivier S, De Ledinghen V, Abergel A, Thabut D, D’Alteroche L, Bouattour M, Asselah T, Ouzan D, Cales P, Chazouillères O, Gelu-Simeon M, Roulot D, Boursier J, Cagnot C, Tamazirt S, Pascale A, Nilusmas S, Lewin M, Ziol M, Carrat F, Duclos-Vallée JC; ANRS CO12 CirVir, CO22 Hepather, and LICAVIR groups. Value of non-invasive test dynamics in guiding HCC surveillance decisions after HCV cure in patients with cirrhosis. J Hepatol. 2025 Sep;83(3):701-711. doi: 10.1016/j.jhep.2025.02.008. Epub 2025 Feb 26. PMID: 40020929.
- Delignette MC, Riff A, Antonini T, Soustre T, Bodinier M, Peronnet E, Venet F, Gossez M, Pantel S, Mabrut JY, Muller X, Mohkam K, Villeret F, Erard D, Dumortier J, Zoulim F, Heyer L, Guichon C, Blet A, Aubrun F, Monneret G, Lebossé F. Individual mHLA-DR trajectories in the ICU as predictors of early infections following liver transplantation: a prospective observational study. Crit Care. 2025 Feb 18;29(1):79. doi: 10.1186/s13054-025-05305-x. PMID: 39966934; PMCID: PMC11834174.
- Block TM, Guo JT, Zoulim F, Rice CM, Thio CL, Schneider WM, Alter HJ, Jacobson IM, Gish RG, Block PD, Sulkowski M, Feld JJ, Cohen CA. New potent HBV replication inhibitors for the management of chronic hepatitis B are needed. Nat Rev Gastroenterol Hepatol. 2025 Mar;22(3):150-151. doi: 10.1038/s41575-025-01037-z. PMID: 39910374.
- Barré T, Ramier C, Ory K, Saidi T, Sogni P, Zoulim F, Bureau-Stoltmann M, Protopopescu C, Marcellin F, Carrieri P; ANRS CO13 HEPAVIH Study Group. Liver Enzyme Elevation After Hepatitis C Virus Cure: Is There a Sex Effect? (ANRS CO13 HEPAVIH Cohort). J Viral Hepat. 2025 Mar;32(3):e70007. doi: 10.1111/jvh.70007. PMID: 39878781.
- Barré T, Ramier C, Wittkop L, Sogni P, Zucman D, Tardieu R, Carrieri P, Marcellin F; ANRS CO13 HEPAVIH Study Group. Low CD4 Cell Count Is Associated With Post-Hepatitis C Virus Cure Mortality in People With HIV (ANRS CO13 HEPAVIH Cohort). Clin Infect Dis. 2025 Sep 16;81(2):e28-e30. doi: 10.1093/cid/ciaf016. PMID: 39812016.
- Degasperi E, Anolli MP, Jachs M, Reiberger T, De Ledinghen V, Metivier S, D’Offizi G, di Maria F, Schramm C, Schmidt H, Zöllner C, Tacke F, Dietz-Fricke C, Wedemeyer H, Papatheodoridi M, Papatheodoridis G, Carey I, Agarwal K, Van Bömmel F, Brunetto MR, Cardoso M, Verucchi G, Ciancio A, Zoulim F, Aleman S, Semmo N, Mangia A, Hilleret MN, Merle U, Santantonio TA, Coppola N, Pellicelli A, Roche B, Causse X, D’Alteroche L, Dumortier J, Ganne N, Heluwaert F, Ollivier I, Roulot D, Viganò M, Loglio A, Federico A, Pileri F, Maracci M, Tonnini M, Arpurt JP, Barange K, Billaud E, Pol S, Gervais A, Minello A, Rosa I, Puoti M, Lampertico P. Real-world effectiveness and safety of bulevirtide monotherapy for up to 96 weeks in patients with HDV-related cirrhosis. J Hepatol. 2025 Jun;82(6):1012-1022. doi: 10.1016/j.jhep.2024.12.044. Epub 2025 Jan 8. PMID: 39793613.
- Barré T, Ramier C, Ory K, Sogni P, Aumaitre H, Saidi T, Carrieri P, Marcellin F; ANRS CO13 HEPAVIH Study Group. Transient CD4 cell recovery after hepatitis C virus cure in HIV/hepatitis C virus coinfected patients (ANRS CO13 HEPAVIH cohort). HIV Med. 2025 Mar;26(3):500-503. doi: 10.1111/hiv.13752. Epub 2024 Dec 11. PMID: 39663177.
- Degasperi E, Scholtes C, Testoni B, Renteria SU, Anolli MP, Charre C, Facchetti F, Plissonnier ML, Sambarino D, Perbellini R, Monico S, Callegaro A, García-Pras E, Lens S, Cortese MF, Forns X, Pérez-Del-Pulgar S, Heil M, Levrero M, Zoulim F, Lampertico P. Differential HBV RNA and HBcrAg patterns in untreated patients with chronic hepatitis delta. J Hepatol. 2025 Jun;82(6):1004-1011. doi: 10.1016/j.jhep.2024.11.051. Epub 2024 Dec 9. PMID: 39662705.
- Roulot D, Layese R, Brichler S, Ganne N, Asselah T, Zoulim F, Gordien E, Nahon P, Roudot-Thoraval F; DeltaVir and CirVir study groups. Hepatitis D Virus Infection Markedly Increases the Risk of Hepatocellular Carcinoma in Patients With Viral B Cirrhosis. Clin Gastroenterol Hepatol. 2025 Oct;23(11):1943-1953.e2. doi: 10.1016/j.cgh.2024.08.046. Epub 2024 Oct 24. PMID: 39461464.
- Parent R, Lin RL, Ouillette L, Glass E, Burns H, Uhler MD, Case SL, Thibault O, Murphy GG. The Impact of Overexpression of the Mouse Ortholog of CACNA1C on Behavior and Cortical Dynamics. Biol Psychiatry Glob Open Sci. 2025 May 22;5(5):100537. doi: 10.1016/j.bpsgos.2025.100537. PMID: 40678692; PMCID: PMC12268564.
- Elzinga SE, Guo K, Turfah A, Henn RE, Webber-Davis IF, Hayes JM, Pacut CM, Teener SJ, Carter AD, Rigan DM, Allouch AM, Jang DG, Parent R, Glass E, Murphy GG, Lentz SI, Chen KS, Zhao L, Hur J, Feldman EL. Metabolic stress and age drive inflammation and cognitive decline in mice and humans. Alzheimers Dement. 2025 Mar;21(3):e70060. doi: 10.1002/alz.70060. PMID: 40110679; PMCID: PMC11923576.
- Meunier L, Delire B, De Martin E, Lebossé F, Anty R, Dumortier J, Houssel-Debry P, Delwaide J, Duclos-Vallee JC, Lutu A, Lemoinne S, Roux O, Péron JM, Saviano A, Abergel A, Prost A, Hountondji L, Thabut D, Dharancy S, Antonini T, Zahhaf A, Horsmans Y, Larrey D; REFHEPS group. Features and Outcomes of 280 Patients With Idiosyncratic Drug-induced Liver Injury: The REFHEPS Prospective Study. Clin Gastroenterol Hepatol. 2025 Nov 4:S1542-3565(25)00933-4. doi: 10.1016/j.cgh.2025.10.024. Epub ahead of print. PMID: 41197933.
- Thévenot T, Elkrief L, Bureau C, Bardou-Jacquet E, Rosa I, Nguyen-Khac E, Oberti F, Pitta A, Mallet M, Lebossé F, Louvet A, Meunier L, Nahon P, Ollivier-Hourmand I, Anty R, Francoz C, Riachi G, Meunier A, Cervoni JP, Tio G, Muller A, Curé-Martin A, Ladeira R, Clairet AL, Hocquet D, Di Martino V, Weil D, Desmarets M. Effect of rifaximin in patients with severe cirrhosis and ascites: A randomized double-blind placebo-controlled trial. J Hepatol. 2025 Dec;83(6):1320-1327. doi: 10.1016/j.jhep.2025.06.019. Epub 2025 Jul 11. PMID: 40653111.
2024
- Chapus F*, Giraud G*, Huchon P, Rodà M, Grand X, Charre C, Goldsmith C, Roca Suarez AA, Martinez MG, Fresquet J, Diederichs A, Locatelli M, Polvèche H, Scholtès C, Chemin I, Vargas HH, Rivoire M, Bourgeois CF, Zoulim F, Testoni Bc. Helicases DDX5 and DDX17 promote heterogeneity in HBV transcription termination in infected human hepatocytes. J Hepatol. 2024 May 21:S0168-8278(24)00351-9. doi: 10.1016/j.jhep.2024.05.016. Epub ahead of print. PMID: 38782119.
- Roca Suarez AA, Plissonnier ML, Grand X, Michelet M, Giraud G, Saez-Palma M, Dubois A, Heintz S, Diederichs A, Van Renne N, Vanwolleghem T, Daffis S, Li L, Kolhatkar N, Hsu YC, Wallin JJ, Lau AH, Fletcher SP, Rivoire M, Levrero M, Testoni BC, Zoulim Fc. TLR8 agonist selgantolimod regulates Kupffer cell differentiation status and impairs HBV entry into hepatocytes via an IL-6-dependent mechanism. Gut. 2024 May 2:gutjnl-2023-331396. doi: 10.1136/gutjnl-2023-331396. Epub ahead of print. PMID: 38697771.
- Giraud G, Rodà M, Huchon P, Michelet M, Maadadi S, Jutzi D, Montserret R, Ruepp MD, Parent R, Combet C, Zoulim F, Testoni Bc. G-quadruplexes control hepatitis B virus replication by promoting cccDNA transcription and phase separation in hepatocytes. Nucleic Acids Res. 2024 Mar 21;52(5):2290-2305. doi: 10.1093/nar/gkad1200. PMID: 38113270.
- Smekalova EM, Martinez MG, Combe E, Kumar A, Dejene S, Leboeuf D, Chen CY, Dorkin JR, Shuang LS, Kieft S, Young L, Barrera LA, Packer MS, Ciaramella G, Testoni B, Gregoire F, Zoulim Fc. Cytosine base editing inhibits hepatitis B virus replication and reduces HBsAg expression in vitro and in vivo. Mol Ther Nucleic Acids. 2023 Dec 27;35(1):102112. doi: 10.1016/j.omtn.2023.102112. PMID: 38292874; PMCID: PMC10825689.
- Meyniel-Schicklin L, Amaudrut J, Mallinjoud P, Guillier F, Mangeot PE, Lines L, Aublin-Gex A, Scholtes C, Punginelli C, Joly S, Vasseur F, Manet E, Gruffat H, Henry T, Halitim F, Paparin JL, Machin P, Darteil R, Sampson D, Mikaelian I, Lane L, Navratil V, Golinelli-Cohen MP, Terzi F, André P, Lotteau V, Vonderscher J, Meldrum EC, de Chassey B. Viruses traverse the human proteome through peptide interfaces that can be biomimetically leveraged for drug discovery. Proc Natl Acad Sci U S A. 2024 Jan 30;121(5):e2308776121. doi: 10.1073/pnas.2308776121. Epub 2024 Jan 22. PMID: 38252831; PMCID: PMC10835127.
- Roca Suarez AA, Planel S, Grand X, Couturier C, Tran T, Porcheray F, Becker J, Reynier F, Delgado A, Cascales E, Peyrot L, Tamellini A, Saliou A, Elie C, Baum C, Vuong BQ, Testoni B, Roques P, Zoulim F, Hasan U, Chemin Ic. Interspecies comparison of the early transcriptomic changes associated with hepatitis B virus exposure in human and macaque immune cell populations. Front Cell Infect Microbiol. 2023 Sep 1;13:1248782. doi: 10.3389/fcimb.2023.1248782. eCollection 2023.PMID: 37727809.
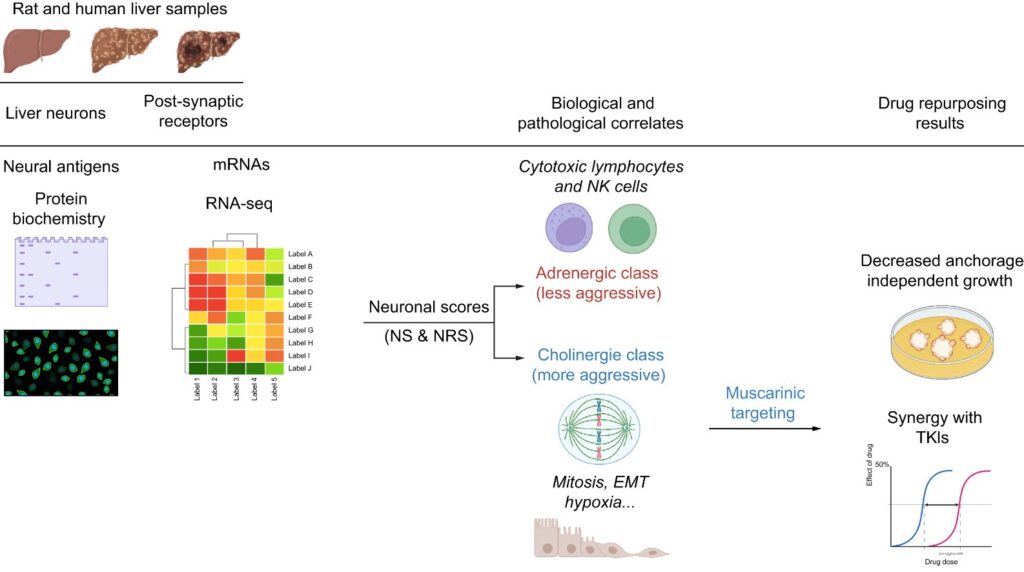
- Hernandez CA*, Verzeroli C*, Roca-Suarez AA*, Farca-Luna AJ, Tonon L, Esteban-Fabró R, Pinyol R, Plissonnier ML, Chicherova I, Dubois A, Bellaud P, Seffals M,Turlin B, Fautrel A, Ichim G, Rivoire M, Passot G, Macek-Jilkova Z, Decaens T,Viari A, Testoni B, Rebouissou S, Llovet JM, Zoulim F, Parent Rc. Hepatocellular carcinoma hosts cholinergic neural cells and tumoral hepatocytes harboring targetable muscarinic receptors. JHEP Rep. 2024 Nov 12;7(1):101245. doi: 10.1016/j.jhepr.2024.101245. PMID: 39717507; PMCID: PMC11663970.
- Paturel A, Casuscelli di Tocco F, Bousquet D, Plissonnier ML, Grand X, Tak H, Berby F, Scholtès C, Testoni B, Zoulim F, Levrero M. A molecular standard for circulating HBV RNA detection and quantification assays in patients with chronic hepatitis B. JHEP Rep. 2024 May 25;6(10):101124. doi: 10.1016/j.jhepr.2024.101124. PMID: 39328324; PMCID: PMC11424956.
- Zakirova NF, Khomich OA, Smirnova OA, Molle J, Duponchel S, Yanvarev DV, Valuev-Elliston VT, Monnier L, Grigorov B, Ivanova ON, Karpenko IL, Golikov MV, Bovet C, Rindlisbacher B, Khomutov AR, Kochetkov SN, Bartosch B, Ivanov AV. Hepatitis C Virus Dysregulates Polyamine and Proline Metabolism and Perturbs the Urea Cycle. Cells. 2024 Jun 14;13(12):1036. doi: 10.3390/cells13121036. PMID: 38920664; PMCID: PMC11201506.
- Grand X, Giraud G, Rifki A, Paturel A, Bousquet D, Roca Suarez AA, Bourgeois C, Levrero M, Zoulim F, Testoni BC.
Bolero: a dedicated workflow to decipher Hepatitis B virus transcriptome from long-reads sequencing method coupled to 5’RACE amplification of transcripts. bioRxiv 2024.09.17.613398; doi: https://doi.org/10.1101/2024.09.17.613398.
- Testoni B, Scholtès C, Plissonnier ML, Paturel A, Berby F, Facchetti F, Villeret F, Degasperi E, Scott B, Hamilton A, Heil M, Lampertico P, Levrero M, Zoulim Fc. Quantification of circulating HBV RNA expressed from intrahepatic cccDNA in untreated and NUC treated patients with chronic hepatitis B. Gut. 2024 Mar 7;73(4):659-667. doi: 10.1136/gutjnl-2023-330644. PMID: 37879886.
- Yu X, Gong Q, Yu D, Chen Y, Jing Y, Zoulim F, Zhang X. Spatial transcriptomics reveals a low extent of transcriptionally active hepatitis B virus integration in patients with HBsAg loss. Gut. 2024 Apr 5;73(5):797-809. doi: 10.1136/gutjnl-2023-330577. PMID: 37968095; PMCID: PMC11041573.
- Molle J, Duponchel S, Rieusset J, Ovize M, Ivanov AV, Zoulim F, Bartosch Bc. Exploration of the Role of Cyclophilins in Established Hepatitis B and C Infections. Viruses. 2024 Dec 25;17(1):11. doi: 10.3390/v17010011. PMID: 39861799; PMCID: PMC11768883.
- Degasperi E, Scholtes C, Testoni B, Renteria SU, Anolli MP, Charre C, Facchetti F, Plissonnier ML, Sambarino D, Perbellini R, Monico S, Callegaro A, García-Pras E, Lens S, Cortese MF, Forns X, Pérez-Del-Pulgar S, Heil M, Levrero M, Zoulim F, Lampertico P. Differential HBV RNA and HBcrAg patterns in untreated patients with chronic hepatitis delta. J Hepatol. 2024 Dec 9:S0168-8278(24)02759-4. doi: 10.1016/j.jhep.2024.11.051. Epub ahead of print. PMID: 39662705.
- Asselah T, Chulanov V, Lampertico P, Wedemeyer H, Streinu-Cercel A, Pântea V, Lazar S, Placinta G, Gherlan GS, Bogomolov P, Stepanova T, Morozov V, Syutkin V, Sagalova O, Manuilov D, Mercier RC, Ye L, Da BL, Chee G, Lau AH, Osinusi A, Bourliere M, Ratziu V, Pol S, Hilleret MN, Zoulim Fc. Bulevirtide Combined with Pegylated Interferon for Chronic Hepatitis D. N Engl J Med. 2024 Jul 11;391(2):133-143. doi: 10.1056/NEJMoa2314134. Epub 2024 Jun 6. PMID: 38842520.
- Chouik Y, Aubin A, Maynard-Muet M, Segrestin B, Milot L, Hervieu V, Zoulim F, Disse E, Levrero M, Caussy C. The grade of obesity affects the noninvasive diagnosis of advanced fibrosis in individuals with MASLD. Obesity (Silver Spring). 2024 Jun;32(6):1114-1124. doi: 10.1002/oby.24033. Epub 2024 May 3. PMID: 38699960.
- Begré L, Boyd A, Plissonnier ML, Testoni B, Salazar-Vizcaya L, Suter-Riniker F, Scholtès C, Béguelin C, Rockstroh JK, Günthard HF, Calmy A, Cavassini M, Hirsch HH, Schmid P, Bernasconi E, Levrero M, Wandeler G, Zoulim F, Rauch A; Swiss HIV Cohort Study. Circulating HBV RNA and hepatitis B core-related antigen trajectories in persons with HIV/HBV coinfection and HBsAg loss on tenofovir therapy. J Infect Dis. 2024 Apr 16:jiae189. doi: 10.1093/infdis/jiae189. Epub ahead of print. PMID: 38626170.
- Ndow G, Vo-Quang E, Shimakawa Y, Ceesay A, Tamba S, Njai HF, Bojang L, Hateley C, Takao Y, Opoku E, Warsop Z, Ingiliz P, D’Alessandro U, Chemin I, Mendy M, Thursz M, Njie R, Lemoine M. Clinical characteristics and outcomes of patients with cirrhosis and hepatocellular carcinoma in The Gambia, west Africa: a prospective cohort study. Lancet Glob Health. 2023 Sep;11(9):e1383-e1392. doi: 10.1016/S2214-109X(23)00263-2.
- Roca Suarez AA, Plissonnier ML, Michelet M, Dubois A, Heintz S, Saez-Palma M, Delphin M, Bordes I, Molle J, Diederichs A, Rodà M, Combe E, Mougené L, Giraud G, Grand X, Rivoire M, Levrero M, Testoni B, Zoulim Fc. Protocol for isolating CD163<sup>+</sup> Kupffer cells from human liver resections. STAR Protoc. 2024 Dec 20;5(4):103359. doi: 10.1016/j.xpro.2024.103359. Epub 2024 Oct 4. PMID: 39368096; PMCID: PMC11491951.
- Parant F, Delignette MC, Charpiat B, Lacaille L, Lebosse F, Monneret G, Mohkam K, Mabrut JY, Aubrun F, Heyer L, Antonini Tc. Tacrolimus Monitoring in Liver Transplant Recipients, Posttransplant Cholestasis: A Comparative Between 2 Commercial Immunoassays and a Liquid Chromatography-Tandem Mass Spectrometry Method. Ther Drug Monit. 2024 Aug 1;46(4):446-455. doi: 10.1097/FTD.0000000000001201. Epub 2024 Apr 19. PMID: 38648663.
- Debsikréo N, Dehainsala M, Debsikréo O, Leye N, Lo G, Dia A, Flore MNB, Diaw NA, Diouf ND, Otchere ID, Toyé RM, Chemin I, Moussa AM, Toure-Kane NC, Lunel-Fabiani F. Prevalence and molecular characterization of hepatitis delta virus infection among hepatitis B virus surface antigen positive students and pregnant women in N’djamena, Chad. IJID Reg. 2024 Dec 28;14:100560. doi: 10.1016/j.ijregi.2024.100560. PMID: 39895833; PMCID: PMC11786080.
- Ndow G, Shimakawa Y, Leith D, Bah S, Bangura R, Mahmoud I, Bojang L, Ceesay A, Drammeh S, Bola-Lawal Q, Lambert G, Hardy P, Ingiliz P, Haddadin Y, Vo-Quang E, Chevaliez S, Cloherty G, Bittaye SO, Lo G, Toure-Kane C, Mendy M, Njie R, Chemin I, D’Alessandro U, Thursz M, Lemoine M. Clinical outcomes of untreated adults living with chronic hepatitis B in The Gambia: an analysis of data from the prospective PROLIFICA cohort study. Lancet Gastroenterol Hepatol. 2024 Dec;9(12):1133-1146. doi: 10.1016/S2468-1253(24)00226-7. PMID: 39521002.
- Ceesay A, Drammeh S, Ndow G, Jallow AOA, Nyang H, Bittaye B, Mendy FS, Secka O, D’Alessandro U, Shimakawa Y, Vo-Quang E, Testoni B, Thursz M, Lemoine M, Chemin Ic. Real-Life Diagnostic Accuracy and Clinical Utility of Hepatitis B Virus (HBV) Nucleic Acid Testing Using the GeneXpert Point-of-Care Test System from Fresh Plasma and Dry Blood Spot Samples in The Gambia. Microorganisms. 2024 Nov 9;12(11):2273. doi: 10.3390/microorganisms12112273. PMID: 39597662; PMCID: PMC11596281.
- Chouik Y, Corpechot C, Francoz C, De Martin E, Guillaud O, Abergel A, Altieri M, Barbier L, Besch C, Chazouillères O, Conti F, Dharancy S, Durand F, Duvoux C, Gugenheim J, Hardwigsen J, Hilleret MN, Houssel-Debry P, Kamar N, Minello A, Neau-Cransac M, Pageaux GP, Radenne S, Roux O, Saliba F, Samuel D, Vanlemmens C, Woehl-Jaegle ML, Leroy V, Duclos-Vallée JC, Dumortier J. Autoimmune hepatitis recurrence after liver transplantation: « Les jeux sont faits ». Liver Transpl. 2024 Apr 1;30(4):395-411. doi: 10.1097/LVT.0000000000000278. Epub 2023 Oct 4. PMID: 37788303.
- Kumar A, Combe E, Mougené L, Zoulim F, Testoni Bc. Applications of CRISPR/Cas as a Toolbox for Hepatitis B Virus Detection and Therapeutics. Viruses. 2024 Oct 2;16(10):1565. doi: 10.3390/v16101565. PMID: 39459899; PMCID: PMC11512240.
- Zoulim Fc. Does siRNA-based therapy require pegylated interferon-alfa-2a to cure HBV infection? Lancet Gastroenterol Hepatol. 2024 Dec;9(12):1069-1071. doi: 10.1016/S2468-1253(24)00303-0. Epub 2024 Oct 8. PMID: 39389080.
- Villeret F, Nahon P. Atezolizumab and bevacizumab with anticoagulant or antiplatelet therapy in hepatocellular carcinoma patients: Real-world data for clinical decision-making. Liver Int. 2024 Aug;44(8):1749-1750. doi: 10.1111/liv.15954. PMID: 39012158.
- Pezy P, Rossignol G, Muller X, Delignette MC, Antonini T, Lebossé F, Mabrut JY, Mohkam K. Two-team Versus Single-team Liver Transplantation. Transplantation. 2024 Nov 1;108(11):e390-e392. doi: 10.1097/TP.0000000000004982. Epub 2024 Oct 22. PMID: 39466198.
- Cocca M*, Testoni B*c. New dimension in viral hepatitis research. eGastroenterology. 2024 Oct 2;2(3):e100136. doi: 10.1136/egastro-2024-100136. PMID: 39944365; PMCID: PMC11731076.
- Tu T, Wettengel J, Xia Y, Testoni B, Littlejohn M, Le Bert N, Ebert G, Verrier ER, Tavis JE, Cohen C. Major open questions in the hepatitis B and D field – Proceedings of the inaugural International emerging hepatitis B and hepatitis D researchers workshop. Virology. 2024 Jul;595:110089. doi: 10.1016/j.virol.2024.110089. Epub 2024 Apr 16. PMID: 38640789; PMCID PMC11517827.
- Giraud G, El Achi K, Zoulim F, Testoni Bc. Co-Transcriptional Regulation of HBV Replication: RNA Quality Also Matters. Viruses. 2024 Apr 16;16(4):615. doi: 10.3390/v16040615. PMID: 38675956; PMCID: PMC11053573.
Membres de l'équipe

Ludovic AILLOT
Post-doctorant - Inserm
Post-doctorant dont les recherches visent à améliorer notre compréhension des interactions entre le système immunitaire de l’hôte et les agents pathogènes. Je mène également des études sur de nouveaux composés innovants stimulant la réponse immunitaire, afin d’évaluer leur potentiel antiviral.

Birke BARTOSCH
Directrice de Recherches - Inserm
Ses thématiques de recherche principales sont les interactions virus-hôte et notamment le rôle des changements métaboliques viro-induits dans les pathologies des hépatites chroniques. Elle a mené de nombreux travaux sur ses travaux sur la pathologie de l’hépatite C chronique.

Isabelle CHEMIN
Directrice de Recherches - Inserm
Depuis plusieurs années, elle se concentre sur les variantes du VHB et le carcinome hépatocellulaire, y compris les marqueurs pronostiques et prédictifs du développement du CHC. Elle a contribué à la mise en place et au développement de plusieurs études collaboratives, notamment avec l’Amérique du Sud, l’Afrique du Nord et l’Afrique de l’Ouest.

Emmanuel COMBE
Ingénieur d’Etudes - Inserm
Au sein de l’équipe du Dr Barbara Testoni depuis 2020, je participe à des projets visant à neutraliser le réservoir du virus de l’hépatite B (cccDNA) à l’aide d’approches innovantes d’édition génomique, notamment CRISPR-Cas9 et les éditeurs de bases cytosine et adénosine, administrées aux hépatocytes par le biais de stratégies cliniquement pertinentes.

Marine DELEUME
Doctorante - Inserm
Pharmacienne biologiste, je réalise un doctorat sur les biomarqueurs non-invasifs et innovants du virus de l’hépatite B (HBcrAg, ARN circulants et variants d’épissage, isoformes de l’AgHBs). J’évalue leur apport diagnostic et pronostic dans les mono et co-infections VHB-VHD, dans une démarche de recherche transversale avec le service de Virologie des Hospices Civils de Lyon. Ces recherches visent à approfondir les connaissances sur ces biomarqueurs et faire avancer la prise en charge des patients infectés ou à risque de réactivation virale par le VHB.

Audrey DIEDERICHS
Ingénieur d’Etudes - UCBL
Je suis ingénieur d’études et je travaille dans l’équipe de Barbara Testoni sur différents projets.
– Test de différents modulateurs d’assemblage de capside (CAM) et leurs impacts sur la réplication du virus de l’hépatite B.
– Test de nouveaux agents thérapeutiques (ASO) contre le virus HBV sur des modèles de cellules primaires tels que les hépatocytes primaires humains (PHH) ainsi que sur des modèles de Precision-cut liver slices (PCLS) afin de mieux comprendre leur mécanisme d’action.

Guillaume GIRAUD
Chargé de Recherches - Inserm
Mes recherches portent sur la compréhension des mécanismes moléculaires contrôlant le métabolisme des ARNm du virus de l’hépatite B (VHB). En particulier, mes projets portent d’une part, sur l’identification de facteurs régulant l’épissage des ARN viraux et d’autre part, sur la contribution des variants d’épissage dans la pathogenèse hépatique induite par ce virus.

Jennifer MOLLE
Ingénieur d'Etudes - Inserm
Je suis ingénieur. Je travaille avec Birke Bartosch sur les interactions métaboliques des protéines mitochondriales avec les virus de l’hépatite B, C et D. Je suis responsable du laboratoire P2 et participe activement à la prévention des risques en tant que responsable de la prévention, contribuant ainsi à la sécurité du laboratoire, à la conformité et aux bonnes pratiques expérimentales.

Léa MOUGENÉ
Doctorante - Inserm
Actuellement doctorante sous la supervision du Dr. Barbara Testoni, je travaille sur l’évaluation des ARNs circulants du VHB dans les vésicules extracellulaires. A terme, mes recherches pourraient mener à la découverte de nouveaux biomarqueurs utiles pour le diagnostic et le suivi de l’hépatite B chronique.

Fanny LEBOSSÉ
MCU-PH
Je suis MCU-PH en hépatologie à l’Université Lyon 1 et aux hospices Civils de Lyon. Je travaille sur les dysfonctions immunitaires associées à la cirrhose depuis 2015, et plus généralement sur les maladies du foie à un stade très avancé. Mes travaux s’intéressent à l’impact de la dysfonction immunitaire de la cirrhose sur le pronostic des patients cirrhotiques, et notamment sur le risque infectieux. L’objectif est de comprendre les mécanismes favorisant les dysfonctions immunitaires pour développer des stratégies visant à réduire le risque infectieux. A l’hôpital, je prends en charge les patients avec une cirrhose sévère et dans un parcours de transplantation hépatique.
En lien avec ces thèmes de recherche, je coordonne et/ou participe à trois études cliniques :
– EmiC : Etude la variance de l’expression des micro-ARN circulants dans une population de patients cirrhotiques en décompensation aiguë. Financement : HCL jeunes chercheurs – IHU Lyon – SNFGE (FARE 2022 et 2025)
– I4 cirrhosis : Impact des modifications de réponse des Lymphocytes T CD4 au cours de l’histoire naturelle de la cirrhose. Financement : HCL jeunes chercheurs – IHU Lyon – SNFGE (FARE 2022 et 2025)
– PREDITH : Développement d’un score PREDictif du risque Infectieux en post Transplantation Hépatique immédiat. Financement : IHU Lyon – PHRCI AURA
Liens vers mes publications récentes :
–https://pubmed.ncbi.nlm.nih.gov/39966934/

Boyan GRIGOROV
Maître de Conférences – UCBL
Maître de conférences en biochimie et biotechnologie à la Faculté de Pharmacie de l’UCBL, je coordonne également le Master Cancer M1. Je suis impliqué dans des programmes internationaux conjoints avec l’USTH (Vietnam) et le VIT (Inde), où j’enseigne la biotechnologie biomédicale au niveau master. Mes recherches portent sur les interactions virus–cellule hôte, avec un intérêt pour l’héparanase-1 et son rôle dans les infections virales. Je dirige un projet évaluant des inhibiteurs de l’héparanase-1 — notamment le mimétique PI 88 — comme antiviraux potentiels contre le VIH 1, le VHB et le VHD. Je mène également un projet sur la protéine CD46 et son implication possible dans les maladies chroniques du foie.

Octavie PARIS
Manager de Projets
Manager de projets européens, elle accompagne depuis plusieurs années le Prof. Zoulim dans la coordination du projet H2020 IP-cure-B Immune profiling to guide host-directed interventions to cure HBV infections en assurant l’animation de ce consortium international comptant 14 institutions partenaires.
Elle est également en charge de l’animation de la Task Force ANRS HBV Cure et a rejoint il y a un an l’équipe de l’Institut Hospitalo-Universitaire (IHU) d’Hépatologie de Lyon en tant que cheffe de projets.

Romain PARENT
Chargé de Recherches - Inserm
Je suis pharmacien chercheur et ai suivi une formation complémentaire en virologie (doctorat). Mon groupe de recherche s’intéresse particulièrement aux maladies chroniques du foie, au cancer du foie et à leur interaction avec les fibres neuronales.
Les projets financés par l’ANRS et l’INCa (Institut national du cancer) constituent actuellement une source importante pour leur mise en œuvre, en lien avec l’histopathologie des tissus concernés, la pharmacologie et la biologie cellulaire. Cependant, nous sommes également heureux de collaborer avec des neuropsychologues tels qu’Emilie Favre (Université Lumière – Lyon 2) afin d’élargir les perspectives actuelles sur les maladies hépatiques vers un ensemble d’approches plus intégrées. Cela se concrétise à travers le projet PsyLiver, financé par SHAPE-Med et coordonné conjointement.

Maud MICHELET
Ingénieur d'Etudes - Inserm
Je suis ingénieur de recherche titulaire depuis 2010 dans le laboratoire du professeur Fabien Zoulim.
Je travaille actuellement dans l’équipe du Dr Barbara Testoni sur différents projets :
– Test de différentes molécules (principalement des modulateurs d’assemblage de capside – CAM) sur la réplication du virus de l’hépatite B.
– Développement de différents modèles de culture cellulaire à partir de foies humains :
- Hépatocytes humains primaires (PHH)
- PCLS (Precision-Cut Liver Slices)
Au sein du laboratoire, je suis responsable, avec le Dr Marie Laure Plissonnier, de la gestion du prélèvement et de l’utilisation des échantillons de tissu hépatique (PHH et PCLS). Nous sommes également responsables de la pièce de culture de niveau 3 (L3) sur site.

Andrea REVILLOT
Ingénieur d'Etudes - Inserm
Je suis ingénieure dans l’équipe du Dr Barbara Testoni. Je travaille sous la supervision du Dr Andres Roca sur la caractérisation de l’effet anti-VHB et immunomodulateur d’un anticorps. Pour cela je caractérise des cellules immunitaire, les lymphocytes T γδ grâce à la cytométrie en flux spectrale et test les effets de l’anticorps sur des hépatocytes infecté par le virus de l’hépatite B.

Maureen RITTER
Post-doctorante - Inserm
Chercheuse en virologie et actuellement en post-doctorat, je m’intéresse aux interactions entre les protéines cellulaires et les protéines virales des virus hépatiques. Mes recherches se concentrent sur la formation du cccDNA du virus de l’hépatite B, processus clé dans l’établissement et le maintien de l’infection.

Armando Andres ROCA SUAREZ
Chargé de Recherches - Inserm
Ses recherches portent sur le développement de modèles ex vivo permettant d’évaluer de nouvelles thérapies ciblant l’hôte contre les infections par le VHB et le VHD. Il s’intéresse également à la biologie des cellules de Kupffer et à l’utilisation de la transcriptomique unicellulaire pour caractériser le microenvironnement hépatique humain.

Coline SEURRE
Doctorante - Inserm
Doctorante en virologie, je m’intéresse à des molécules avec un potentiel antiviral et réalise ma thèse sous la direction du Dr. Boyan Grigorov. Mes recherches portent sur l’étude de l’héparanase-1 dans les cycles viraux du VIH-1 et du VHB et l’évaluation d’inhibiteurs de l’héparanase comme antiviraux potentiels contre ces infections.

Rucha THIGALE
Doctorante - Inserm
Je suis doctorant et mes travaux portent sur l’étude des variants d’épissage de l’ARN du virus de l’hépatite B. Je vais étudier comment ces variants d’épissage contribuent à la pathogenèse hépatique.

Barbara TESTONI
Directrice de Recherche - Inserm
Ses recherches portent principalement sur l’étude des mécanismes épigénétiques à la base de la régulation des gènes de l’hôte et du virus au cours de l’infection par le VHB, avec un accent particulier sur la régulation transcriptionnelle du minichromosome du VHB. Elle participe également à des études translationnelles visant à comprendre les relations entre la persistance du VHB et les perturbations de l’immunité innée intrahépatique et à caractériser de nouveaux biomarqueurs sériques pour l’activité de l’ADNccc intrahépatique.

Fabien ZOULIM
Professeur des Universités - Praticien Hospitalier (UCBL - HCL)
Il s’intéresse aux hépatites virales chroniques et principalement à l’hépatite B, qui demeure un problème majeur de santé publique mondiale avec plus de 250 millions de porteurs chroniques. Les infections chroniques par le virus de l’hépatite B (VHB) représentent la première cause de carcinome hépatocellulaire, deuxième cancer le plus mortel à l’échelon mondial.
Il a développé une expertise dans le domaine de l’hépatite B pour comprendre les mécanismes de persistance virale dans des modèles expérimentaux, identifier de nouvelles cibles antivirales et de nouveaux biomarqueurs prédictifs de réponse aux traitements antiviraux, et évaluer l’efficacité de ces nouveaux traitements dans des essais cliniques.
